《无菌医疗器械包装:标准体系与检测项目全解读》
无菌医疗器械包装:守护生命健康的“无菌屏障系统”
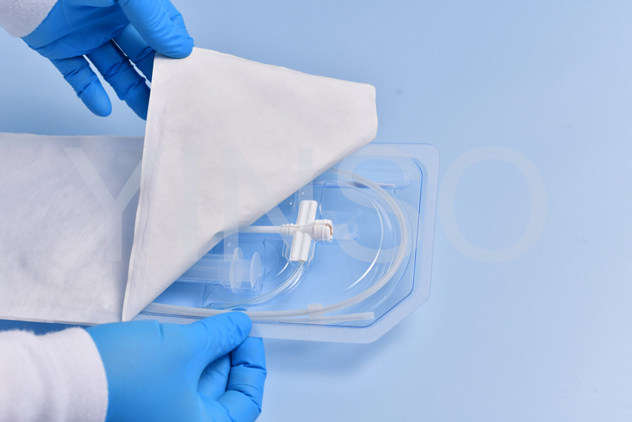
无菌医疗器械包装是保护医疗器械、预防感染的最后一道防线。包装一旦失效,将对患者和医护人员的
健康与生命构成严重威胁。无菌医疗器械包装在专业上也称为“无菌屏障系统”。
与食品行业的无菌包装不同,医疗器械无菌包装不仅要具备阻隔微生物的屏障能力,还必须确保器械在
灭菌后能够在规定期限内维持无菌状态,并能耐受环氧乙烷、伽马辐照、等离子过氧化氢、蒸汽等多种
灭菌方式。正因如此,无菌医疗器械包装被视为医疗器械的一个有机组成部分。
无菌医疗器械国内外标准
我国无菌医疗器械的发展已走过30余年,早期无菌医疗器械包装领域相对滞后。
2005年,我国等同采用ISO 11607-1997,发布了GB/T 19633-2005《最终灭菌医疗器械的包装》。
该标准的发布标志着我国无菌医疗器械包装标准体系的正式建立,极大推动了行业的快速发展。
1. 国外常用标准
国际上通用的纲领性标准为ISO 11607系列,分为两个部分:
ISO 11607-1:材料、无菌屏障系统和包装系统的要求;
ISO 11607-2:成型、密封和装配过程的确认要求。
此外,欧盟发布的EN 868系列以及ASTM系列也是常用标准。比较典型的试验方法标准包括:
ASTM F1980-21《无菌屏障系统和医疗器械加速老化指南》
ASTM F88/F88M-23《柔性阻隔材料密封强度测试方法》
ASTM F1929-2015《多孔医疗包装密封泄漏检测方法(染料法)》等。
2. 国内常用标准
2005年等同采用ISO 11607-1997发布GB/T 19633-2005后,我国陆续转化了ASTM等试验方法
标准,形成了YY/T 0681和YY/T 0698系列标准。随着国际标准的更新,目前GB/T 19633
已随之更新为两部分:
GB/T 19633.1-2024《最终灭菌医疗器械包装 第1部分:材料、无菌屏障系统和包装系统的要求》
GB/T 19633.2-2024《最终灭菌医疗器械包装 第2部分:成形、密封和装配过程的确认要求》
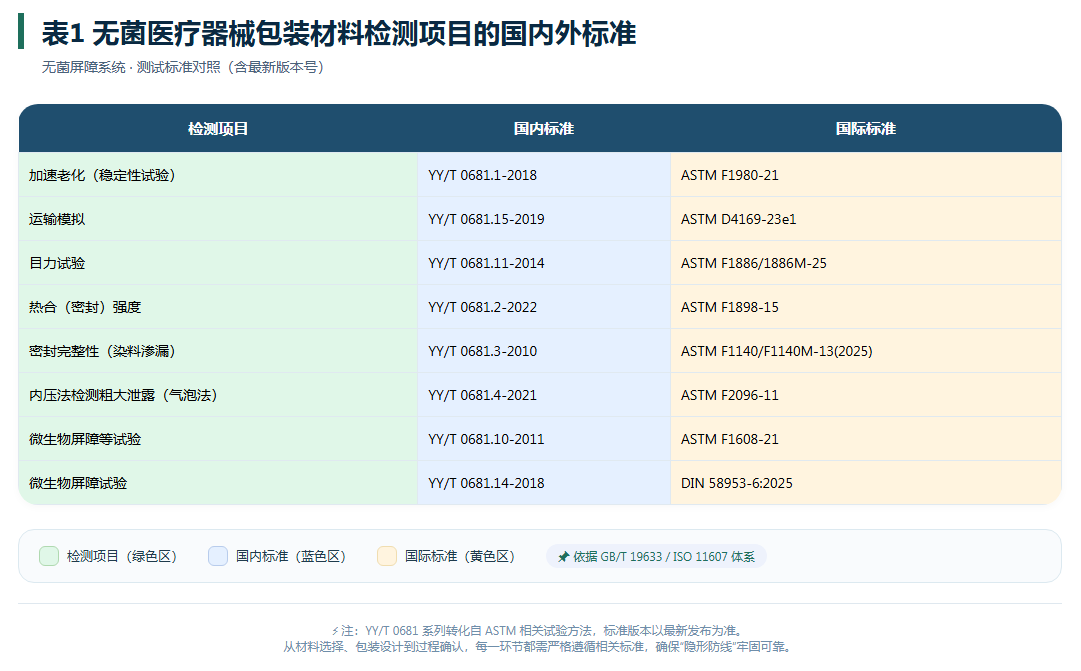
常用包装材料与检测标准对照
目前行业中广泛使用的无菌医疗器械包装材料主要包括:特卫强(Tyvek)、PE/PET复合
膜、吸塑盒等。针对这些材料,国内外测试参考使用的标准通常如下表所示。
结语
从材料选择、包装设计到过程确认,每一个环节都需要严格遵循相关标准,确保这道“隐形防线”
牢固可靠。无菌医疗器械包装看似简单,实则承载着医疗安全的重任。标准体系的建立与持续完善,
正是守护这条生命防线的坚实基础。
——责任编辑:英硕包装
版权所有http://www.yinso.com.cn转载请注明出处
相关推荐:
最新产品
同类文章排行
- 《无菌医疗器械包装:标准体系与检测项目全解读》
- 重磅解读 | 医疗器械初包装微粒污染怎么测?新国标来了!附英硕包装实战经验
- 2026无菌医疗器械常用包装材料与包装形式灭菌方式指南
- 深度解读|2026版《医疗器械生产质量管理规范》新旧对比
- 影响环氧乙烷灭菌效果的因素
- 无菌包装材料的评估项目及测试方法参考
- 影响医疗器械货架有效期的因素
- 《医疗器械初包装的生产环境要求》
- 《最终灭菌医疗器械包装合规标准参考》
- 疫情期间,医用吸塑托盘整柜发往国外
最新资讯文章
您的浏览历史








 粤ICP备14050553号-1
粤ICP备14050553号-1