推荐产品
联系英硕医用包装
定制热线:15016844550
投诉建议:400-998-2901
电话:0769-85602287
传真:0769-85602207
QQ:2850517805
邮箱:yinso6@163.com
地址:东莞市大岭山镇梅林路59号
-
-
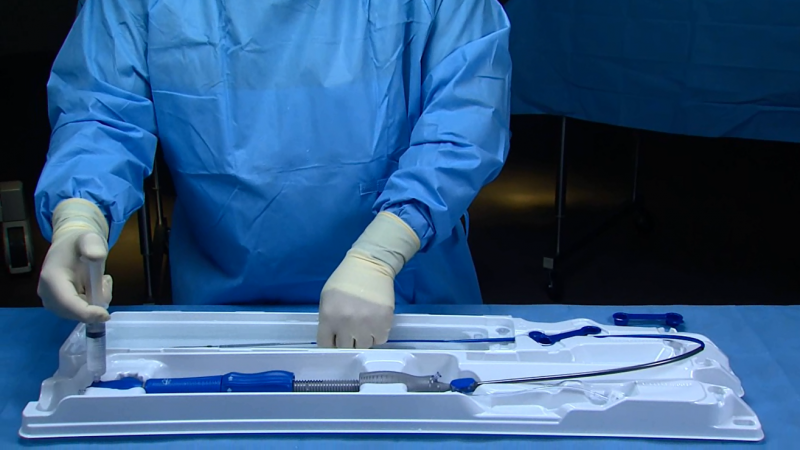
医用吸塑盒厂家解读:为什么三类植入器械必须采用双层无菌屏障系统?
作为医用吸塑盒生产厂家,我们经常被问到:为什么三类植入物一定要用双层无菌屏障系统?今天,我们就从法规分类、风险等级、包装标准三个维度,为您详细解析背后的逻辑。
-
-
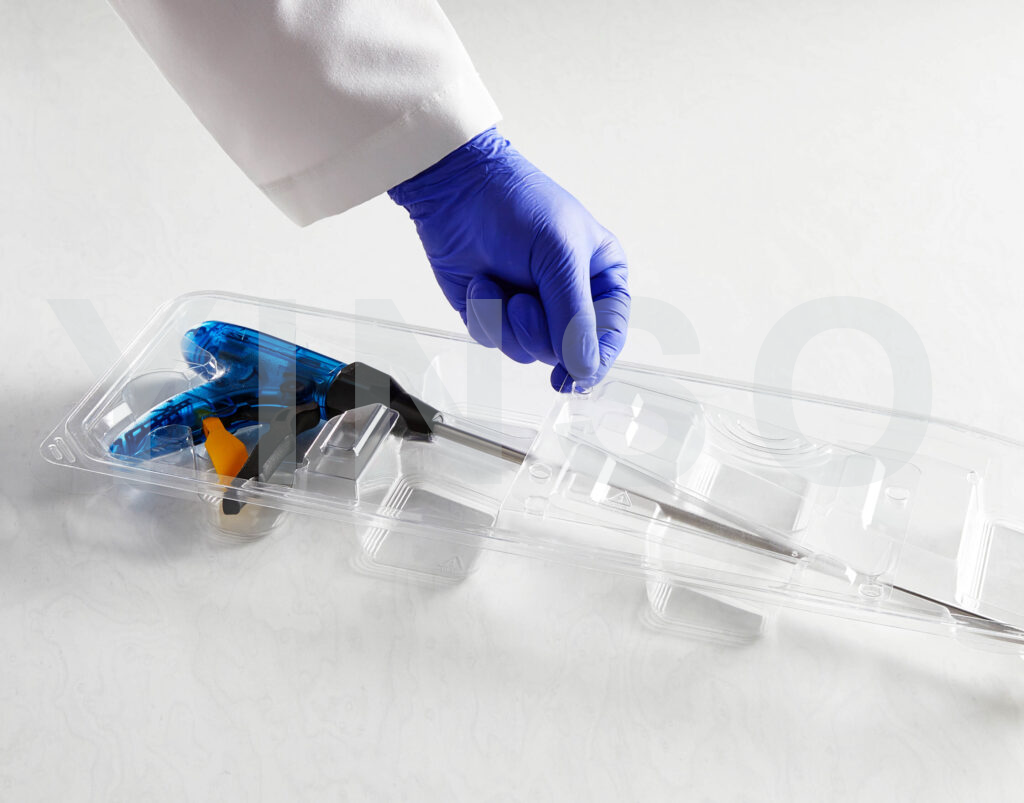
医用吸塑包装热封失效原因解析
在医用吸塑包装领域,包装不仅是产品的“外衣”,更是保障患者安全的无菌屏障系统(Sterile Barrier System, SBS)。它确保医疗器械和药械结合产品从生产到使用的全生命周期内保持无菌状态,防止污染和二次伤害,是医疗安全的第一道防线
-

-
吸塑包装上的“小孔”是干嘛的?揭秘医用泡壳的6个设计细节
拆开灭菌医疗器械时,你是否注意过吸塑包装上的小孔或一些其它细节?它们看似不起眼,却是确保医疗安全的关键设计!
-

-
医用吸塑盒染料渗透测试您了解多少?
在医疗吸塑包装行业中,染料渗透测试是验证包装密封完整性的关键检测方法,用于识别吸塑盒是否存在微孔、裂纹或密封不良等问题,确保医疗器械或药品的无菌性和阻隔性。以下是关于吸塑盒染料渗透测试的详细解析及优化建议:
-

-
医疗器械产品规格型号多?医用吸塑盒兼容设计帮您节省成本
医疗器械产品型号规格多,担心定制医用吸塑盒的时候要开多套模具,前期投入成本太大?英硕包装有妙招!
-
-
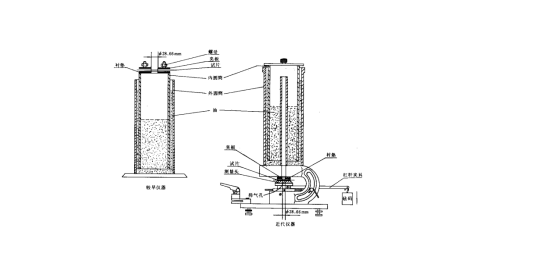
无菌屏障系统不透气材料测试参考标准
无菌屏障系统是无菌器械安全性和有效性的基本保证。而微生物屏障是在考虑了灭菌过程、搬运、运输及贮存等条件后所测试的无菌屏障系统防止微生物进入的性能。
-

-
不同维度来了解医用吸塑盒与普通吸塑盒的差别
医疗吸塑盒作为一道无菌屏障系统更是一道生命屏障,从包装材料的选择、结构设计、模具选择、工艺成型、环境控制、品质监控及包装验证等都至关重要。
-

-
医用硬质吸塑盒的材质选择简述
在介绍医用硬质吸塑盒的材质之前,先简单概括一下吸塑盒的成型原理:吸塑热成型的原理是将成卷的片材拉进电炉烘箱内加热至软化状态,趁热再拉到吸塑模具上方,模具上移并抽真空,将软化的片材吸附到模具表面。同时将冷却水以雾状喷于成型片材表面,使其硬化,成型的片材再自动被拉至贮料箱,气动裁刀将成型与未成型片材分离,从而完成整个吸塑成型过程。
-
-
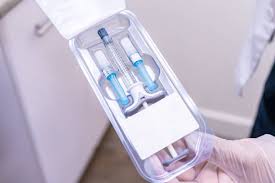
医疗器械包装验证的内容和方法参考
评价微生物屏障特性的两种方法:不透性材料的方法和多孔透气材料的方法。
-

-
最终医疗器械包装评审需注意些什么?
美国FDA缺陷确认研究表明超过50%的涉及无菌医疗器械的召回事件中都与医疗器械包装的质量相关。
-
-
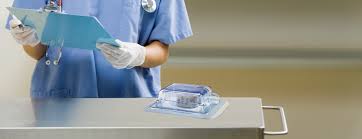
医用吸塑盒设计过程当中,应当注意些什么?
我们曾多次在文章中提及最终灭菌医疗器械包装设计当中应考虑的因素,包括但不限于,如:
-

-
医疗器械常见的包装方式医用硬质包装加盖材
近年来,随着我们的医疗设施不断完善,医疗器械行业不断发展,企业也对包装水平提出了越来越高的要求。医用硬质包装这种密封性好,携带方便,对产品的保护,易于洁净开启适用于灭菌,保持无菌性和完整性的包装方式越来越受到医疗器械公司的亲睐。
-

-
如何给医疗器械选择合适的包装
医疗器械产品包装的选择有很多,但是效果功能却不能同一而论,包装形式的选择,不仅在包装方式上而且在包装设计、灭菌方式、等其他方面的选择方式也是多式多样的。
-

-
关于医疗包装定制PET能否与特卫强热封的问题
众所周知,医疗包装定制材料主要分为PET和PETG,PET颜色主要以透明为主PETG以淡蓝为主,两种材料之间做比较,医疗首选PETG。目前最知名的医用PETG材料供应商主要有两个大公司,韩国SK和美国伊士曼。
-

-
医用纸塑包装的组成结构和使用时注意事项
纸塑包装袋一般由两面组成,一面是透过和排放灭菌因子的纸,常见特卫强纸或透析纸。另一面是不能渗透液体、空气和气体的透明复合薄膜(塑料膜)或者硬吸塑托盘构成。消毒因子的交换在纸的一侧进行,由于材料的原因,同样具有良好的微生物屏障功能,而且塑面对包内物品可视,使包装物品一目了然和具有良好的抗渗能力。
-

-
最终医疗器械包装材料的基本要求
用于最终医疗器械的包装,可对其进行灭菌,可进行无菌操作(如洁净开启),能提供可接受的微生物阻隔性能,灭菌前后能对产品进行保护并且灭菌后能在一定期限内维持系统内部无菌环境的包装系统。
-

-
医疗器械包装密封不严原因剖析
医用透析纸一般是指医学专业特殊材料组成:美国杜邦医用纸+医用涂层,与吸塑包装上的应用,以简洁的外光、优良的微生物阻隔性及易于拿取等优势,成功抢占了医用包装的市场。
-
-
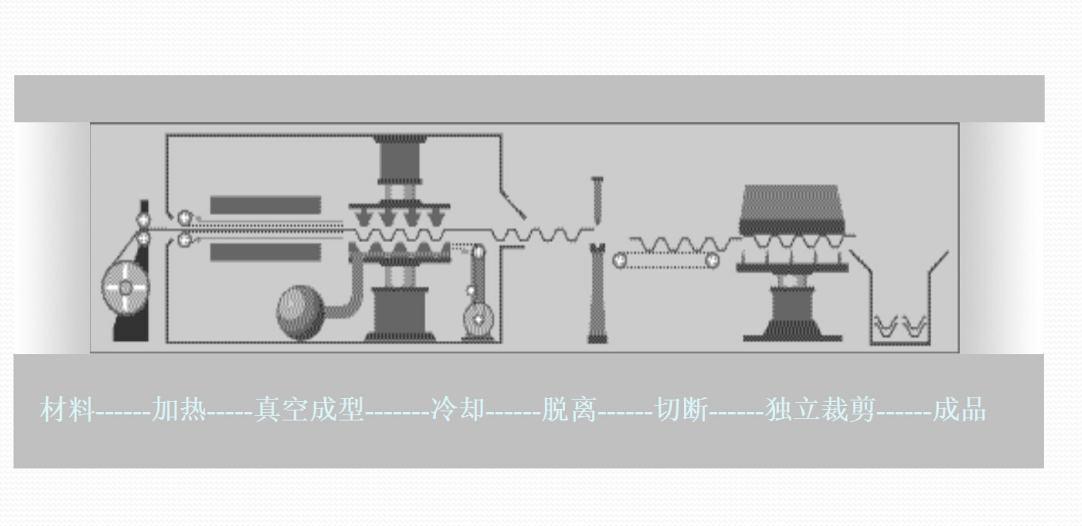
凹凸有致的吸塑成型工艺
吸塑成型又名真空热压成型,吸塑成型的原理是:将成卷的片材拉进电炉烘箱内加热至软化状态,趁热再拉到吸塑模具上方,模具上移并抽真空,将软化的片材吸附到模具表面,待冷却成型后使其硬化。最终成型的片材再自动被拉至贮料箱,气动裁刀将成型与未成型片材分离,从而完成全部过程。
-
-
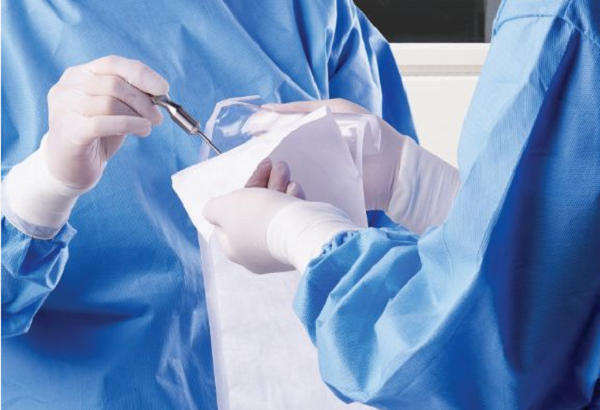
常见的两种无菌屏障系统
严格的无菌屏障系统是需要完整的包装设计方案、包装验证方案和一系列必须的包装实验方案来证明该包装系统就是一个合格的无菌屏障系统。因为SBS是最终灭菌医疗器械安全性的基本保证。
-

-
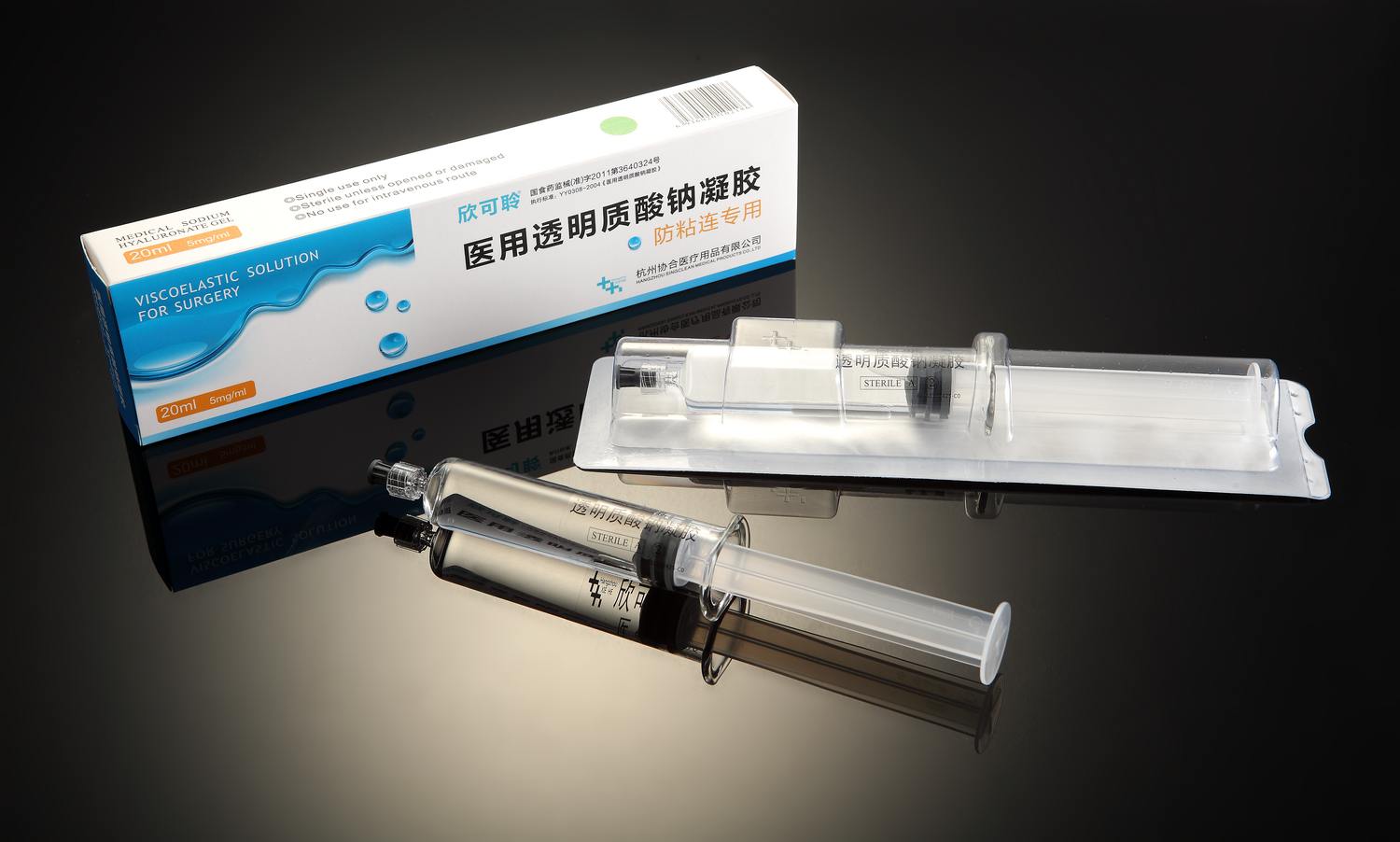
无菌包装设计的基本要求
无菌包装是指具有微生物屏障性能,确保灭菌后能在一定期限内维持器械的无菌状态,可对其灭菌处理,安全开启使用的器械包装。那么无菌包装在设计的时候有什么基本要求呢?










 粤公网安备 44190002005415号
粤公网安备 44190002005415号